私たちの細胞内で日々作られるmRNAは、必要なタンパク質を合成し終えるとただ分解されて「消えていく」もの——そう考えるのが当たり前でした。
ところが日本の東京大学(UTokyo)で行われた研究によって、この“消えていくはず”のmRNAの断片が、なんと同じ遺伝子の転写を抑え込む合図になっていることが明らかになりました。
言い換えると、使い終わったmRNAがただの“廃棄物”ではなく、遺伝子発現を制御する一種の「指示書」に変わるのです。
いったい、細胞はどのようにして自分でつくったmRNAの“消えゆく過程”を転写レベルの調整にまで結びつけているのでしょうか?
研究内容の詳細は『Nucleic Acids Research』にて発表されました。
目次
- mRNAは使い捨てか?常識を覆す新展開
- 切り刻む瞬間こそが勝負!mRNA崩壊から始まる転写制御
- 分解は終わりじゃない:転写のスイッチを握る“mRNAの切れ端”
mRNAは使い捨てか?常識を覆す新展開
私たちの細胞内で繰り広げられている「遺伝子(DNA)からmRNAがつくられ、mRNAがタンパク質を合成し、役目を終えたmRNAは分解されて消えていく」という流れは、あたかも工場の製造ラインのようだと長らく考えられてきました。
製品を作るための設計図(mRNA)は一度使ったら捨てるだけ——そんな“使い捨ての青写真”というイメージが定着していたのです。
ちょうど、完成した製品の図面を処分するように、役目を終えたmRNAは細胞内の分解システムによって粉々にされて消滅する――それでおしまい、という認識が広く共有されてきました。
しかし近年、そうした「使い終わった設計図をそのまま破棄するだけ」という常識に一石を投じる研究報告が、世界各地で相次いでいます。
動物や酵母の細胞を調べた事例からは、“分解途中”のmRNA断片が逆に遺伝子の発現量をコントロールする鍵になっているかもしれない、と示唆する興味深い結果が得られているのです。
まるで廃棄したはずの図面の切れ端が、再び重要な指令書として浮上してくるかのような発見といえるでしょう。
植物の世界も例外ではありません。
土壌に含まれる養分や水分、金属イオンといった多様な環境要因に応じて、柔軟に遺伝子の働きを切り替える巧妙さは、植物が“動けない”なりに生存戦略を磨いてきた証です。
この中でも特に注目される元素がホウ酸(B(OH)₃)などの形で存在するホウ素。
適量がないと細胞壁をうまく形成できず、逆に多すぎると毒にもなるという「必要不可欠だが扱い方を間違えば危険」という両刃の剣のような存在です。
植物にとって、ホウ素が足りなければ必死に取り込み、多すぎれば取り込みを抑える必要があります。
そして、その最前線で働くのがNIP5;1という遺伝子です。
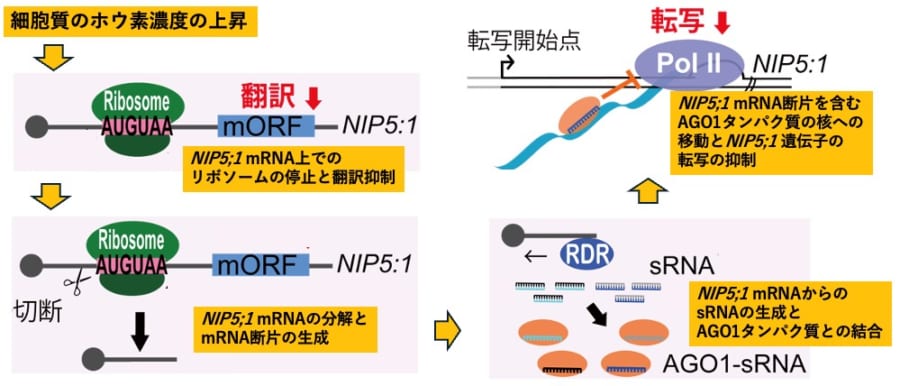
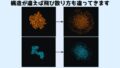
このNIP5;1は主にホウ酸を透過させるためのゲート役を担い、mRNA(転写産物)の5’UTR部分には「リボソームの進行をピタッと止める」特殊な配列が備わっています。
ホウ素が過剰なときには「これ以上はいらない」という判断のもと、リボソームを止めてmRNAを切り刻んでしまうのです。
しかし、このとき生じる“粉々になったmRNAの断片”が、ただ捨てられているのかどうかは長く不明でした。
近年、シュレッダーにかけた文書の切れ端が別の命令書として活用されるように、mRNAの分解過程が細胞内部の新たな仕組みを動かす手がかりになるかもしれない、という可能性が浮上してきました。
つまり、mRNAが「消えていく」その過程がなんと転写(DNAから新たなmRNAをつくる)を抑制する合図になっているかもしれない、というわけです。
東京大学などの研究グループは、この仮説を裏付けるために「ホウ素が豊富な環境下でNIP5;1 mRNAが分解される様子を追跡し、そこで生まれる断片がどのように転写を抑え込むのか」を詳細に調べ始めました。
切り刻む瞬間こそが勝負!mRNA崩壊から始まる転写制御
まず研究チームは、“どのような状態でNIP5;1のmRNAがどれくらい生産され、どのように壊されているのか”を正確に調べるため、ホウ素濃度を変えた培地でシロイヌナズナを育てました。
これは、人間にたとえれば「ミネラル配合が違う食事」を与えるようなもので、低ホウ素と高ホウ素、それぞれ極端な環境を用意することによって、NIP5;1がどのように振る舞うかを比較しやすくしたのです。
時間ごとにmRNA量や分解の状態を測定し、「ホウ素が少ないときにはNIP5;1 mRNAが増えるが、多いときには急に分解される」という変化をリアルタイムで捉えました。
分解の“決定的瞬間”を突き止めるために、研究者たちは複数の分子生物学的手法を組み合わせています。
たとえば「プライマーエクステンション」や「3’RACE」では、mRNAの末端がどこで切れているのかを調べることができます。
これによって、「この位置でmRNAが切断され、断片が生じている」という地図上の座標のような情報が得られるわけです。
また、「smFISH(単一分子蛍光 in situ ハイブリダイゼーション)」という先進的な観察法を使って、細胞内でmRNAがどこに存在するか、どのくらい蓄積しているかも可視化しました。
イメージとしては暗い倉庫に蛍光タグ付きの荷物がいくつあるかを懐中電灯で探すようなもので、“どこで合成が盛んか”“どこで分解が進んでいるか”を精密に確認できるのです。
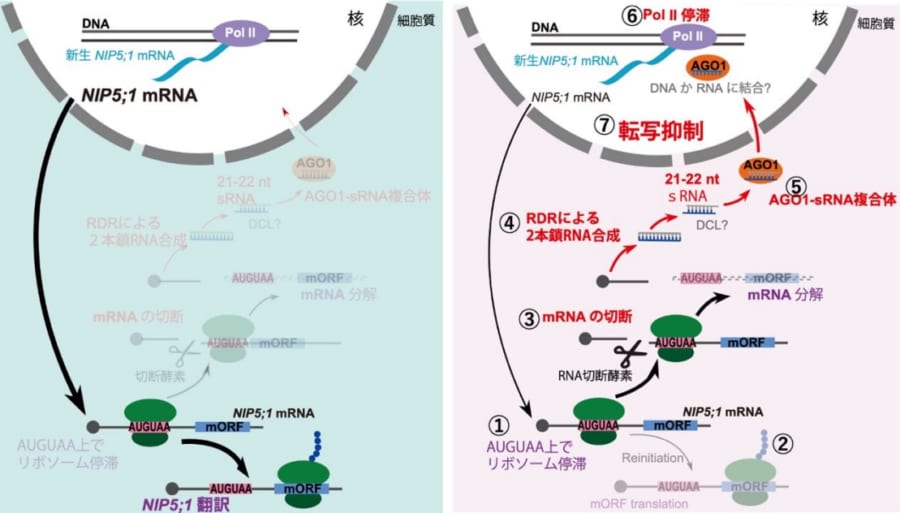
こうした取り組みの中でも特に目を引いたのは、ホウ素が豊富な状態になるとNIP5;1のmRNAがリボソーム(タンパク質合成の工場)の動きをピタッと止められたうえで大胆に切り捨てられ、その断片が「もうNIP5;1を作らなくていい」というシグナルを細胞内に伝えている可能性が高い、という点です。
具体的には、切り刻まれたmRNAのかけらがさらに小さいRNA片に加工されて、ARGONAUTE1(AGO1)などと組み合わさり、核の中へ運ばれていきます。
そこでDNAの転写、つまり“新しいmRNAをつくる作業”をブロックすることで、NIP5;1の生成そのものを止める——いわば細胞全体に「作業ストップ!」と号令をかける役目を果たしているのです。
このメカニズムは、工場ラインの例えで言うと、途中で不良品を廃棄するだけでなく、その廃棄をきっかけに「これ以上の生産をやめよう」という全体指令を発するイメージに近いでしょう。
mRNAは使われ終わったら消えていくはずなのに、その“消える瞬間”を逆手にとって遺伝子の転写段階まで抑え込むわけです。
「mRNA分解=ただの廃棄処分」という従来の見方を覆す、大きな発見と言えます。
分解は終わりじゃない:転写のスイッチを握る“mRNAの切れ端”
今回の結果からわかるのは、“mRNAが壊される”という現象自体が細胞内の重要な指令発信に組み込まれている、という新しい視点です。
普通、分解は使い終わった分子を処分するだけの工程だと考えがちですが、NIP5;1の場合はむしろ分解のプロセスこそが「転写を止める」合図になっている可能性が見えてきました。
こうした“分解と制御の表裏一体”という仕組みは、植物が環境変化に敏感に対応するための合理的な戦略の一つとも考えられます。
ホウ素が急激に増えてしまったとき、あふれる前にNIP5;1 mRNAを切り捨てるだけでなく、その断片からも「もう作らなくていい」というシグナルを発して遺伝子の転写を強力にダウンさせるわけです。
さらに、このような分解によるフィードバックはNIP5;1にとどまらず、ほかの遺伝子や生物系でも起こる可能性が指摘されています。
RNA干渉(RNAi)の仕組みを想起させる点が多く、応用すればウイルスや病原体の遺伝子発現を抑える研究にもつながるかもしれません。
ただし、今回の研究が直接ほかの遺伝子にも当てはまるのかはまだ不確定で、今後の検証が待たれるところです。
それでも、「mRNAは消えて終わりではなく、最後の断片まで情報を使い切る」という細胞の徹底ぶりには驚かされます。
私たちがこれまで思い描いてきた“遺伝子発現の流れ”は、実はもっと奥深く、まだ見ぬ謎が潜んでいるかもしれません。
参考文献
mRNAは消えて終わりじゃない! -mRNA分解中間体が転写を抑える新たなフィードバック機構の発見-
https://www.omu.ac.jp/info/research_news/entry-16781.html
元論文
Ribosome stalling-induced NIP5;1 mRNA decay triggers ARGONAUTE1-dependent transcription downregulation
https://doi.org/10.1093/nar/gkaf159
ライター
川勝康弘: ナゾロジー副編集長。 大学で研究生活を送ること10年と少し。 小説家としての活動履歴あり。 専門は生物学ですが、量子力学・社会学・医学・薬学なども担当します。 日々の記事作成は可能な限り、一次資料たる論文を元にするよう心がけています。 夢は最新科学をまとめて小学生用に本にすること。
編集者
ナゾロジー 編集部