タンパク質を“爆発”させる……一見すると物騒な言葉ですが、実はこれが最新の構造生物学の新しいトレンドだとしたら驚きませんか。
X線レーザーをほんの一瞬照射するだけで、タンパク質は大量の電子を失い、原子どうしが強烈に反発し合って弾け飛びます。
スウェーデンのウプサラ大学(UU)で行われた研究によって、この爆発での破片の飛び散り方を解析すれば、似たように見えるタンパク質でもわずかな折りたたみの違いまで識別できる可能性が示されました。
CERNなどで行われている粒子衝突実験のタンパク質版とも言えかもしれません。
結晶化の難しさや回折データの取得といった従来の壁を越えるかもしれない、この斬新な手法はいったいどのようにして分子の秘密を解き明かすのでしょうか?
研究内容の詳細は『Physical Review Letters』にて発表されました。
目次
- 結晶化から爆発へ、タンパク質構造解析の発展
- 花火のように散る破片が語る、タンパク質の姿
- 壊れる瞬間から逆算する、分子の真実
結晶化から爆発へ、タンパク質構造解析の発展

かつてタンパク質の姿を調べるときには、まず“きれいな結晶”を作ってからX線を当て、回折パターンを見て構造を推定する、というのが王道でした。
でも実際には、いくら待っても結晶ができないタンパク質や、大きすぎたり柔軟に動きすぎたりする分子がたくさんあります。
たとえば、あたかも折り紙をぴったり正方形にたたんでから模様を映し出すような手順が必要で、ちょっとでも形が崩れていると全然うまくいかない、というイメージです。
これが結晶化の壁。
ここでつまずいて、タンパク質の秘密にたどり着けないままという研究者も少なくありませんでした。
その壁を壊すために登場したのが“単粒子イメージング(SPI)”という、まるで舞台の照明を一瞬だけ強烈に当てて、俳優が存在することをかろうじて観測する、みたいな手法です。
ただこの手法は結晶化こそいらないものの、今度は超高強度のX線を当てると、タンパク質自身が壊れてしまうという問題が発生します。
しかし近年、「そのバラバラになる瞬間を、むしろ逆手に取ろうじゃないか」という発想が生まれました。
具体的には、超強力なX線が当たると、タンパク質の原子は大量の電子を奪われて正電荷を帯び、原子どうしが弾けるように飛んでいく――いわゆる“クーロン爆発”が起きます。
ですが解析技術の進歩により、その破片がどの方向へ飛んでいくかを地図のように記録し、いくつも比較するだけで、意外なほど豊富な情報が得られるのではないか、というアイディアが現実味を帯びてきました。
ある意味、これは「分子のレベルで行う粒子衝突実験」ともいえます。
巨大な粒子衝突器では陽子や重イオンを衝突させ、飛び散った破片の痕跡を分析することで物質の根源や新しい粒子を探ります。
それと似たように、ここではタンパク質をX線レーザーで“衝突”させて生じる破片――イオンが飛び散る方向や強度分布――を注意深く解析することで、分子の姿やわずかな構造の違いまで明らかにしようとしているのです。
大きな加速器が巨大な衝突の舞台なら、クーロン爆発は“超小型の衝突劇場”というイメージかもしれません。
飛び散る破片を追うことで、見えなかったタンパク質内部の秘密を解き明かすアプローチは、まさに衝突実験から多くを学ぶ高エネルギー物理の手法と通ずるところがあります。
実際、リゾチームなどを対象に行われたシミュレーション研究では、爆発のパターンからタンパク質の向きや姿勢を推定できる可能性が示されています。
とはいえ、配列が似ているタンパク質同士、あるいは全く同じタンパク質でも折りたたまれ方が少し違うもの(ちょうど腕を伸ばしたポーズと縮こまったポーズのような差)、さらには同じ配列・ほぼ同じ形の二量体といった“そっくりさん”同士まで本当に見分けられるのか。
これは、双子の赤ちゃんを遠目に見ると区別がつかないのに、少し近づくと「あれ、こっちは眉毛がちょっと違う」と気づくようなもの。
こうした細かい差まで爆発パターンで見分けられるのかは未知の領域でした。
そこで今回研究者たちは、あえて「似た構造や配列を持つ複数のタンパク質」に狙いを定めて、爆発から生まれる“フットプリント”(飛び散りの分布)だけを頼りに、どこまで区別できるかを徹底的にシミュレーションで検証することにしたのです。
花火のように散る破片が語る、タンパク質の姿
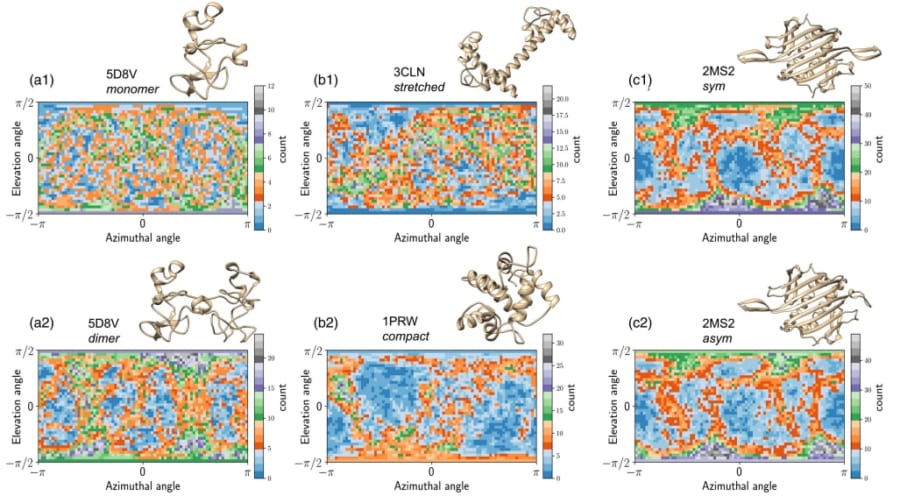
この研究では、タンパク質同士のわずかな違いを「クーロン爆発の仕方」で見分けられるかどうかを確かめようと、まず複数の“そっくりさん”タンパク質を用意しました。
たとえば、「同じタンパク質が1つだけある状態」と「2つくっついている状態」だったり、「アミノ酸配列は同じだけど折りたたみがちょっと違う形」だったり、双子や三つ子といった“兄弟分子”をあえて選んだわけです。
どれもパッと見にはほぼ同じに見えるので、果たして爆発させるだけで区別なんかできるのか、とても不思議に感じるかもしれません。
とはいえ、実際に巨大な装置を使って分子を本当に爆発させるのは手間もコストもかかります。
そこで研究チームは、スーパーコンピュータ上で「超強力なX線レーザーをタンパク質に当てたらどう弾け飛ぶのか」を緻密にシミュレーションすることにしました。
イメージとしては、花火の打ち上げをCGで再現するような感じです。
花火も、火薬の量や玉の作り方が少し違うだけで、夜空で散る色や形が変わりますよね。
それと同じように、タンパク質でも内部の構造や原子の配置がちょっと違うだけで、弾け飛ぶ方向や強さにわずかな差が現れるはずだ—という考えです。
具体的には、高エネルギーのレーザー光子を浴びせることで、タンパク質の原子が大量の電子を奪われ、分子全体が急激に正に帯電します。
すると原子同士が強い斥力で一気に弾き合い、四方八方へ“パッ”と吹き飛ぶのです。
研究者たちは、その飛び散った“破片”がどの方向へ向かったかを、あたかも地図のように記録するプログラムを作り、何百回もの爆発シミュレーションを繰り返して「破片の分布パターン」を大量に集めました。
このパターンこそがいわゆる「爆発フットプリント」で、まるで花火写真を何枚も撮りためて、それぞれの光の散り方を比べるようなものです。
次に、その膨大なフットプリントのデータを一つひとつ解析して、果たして同じタンパク質なら似たパターンになるのか、違うタンパク質なら異なるパターンを示すのかを確かめます。
たとえば、PCA(主成分分析)やt-SNEといった方法でデータを“見える化”すると、特徴が似ているパターンは画面上で近い場所にまとまり、特徴が違うパターンは自然と離れた位置に配置されます。
そのおかげで、それぞれのタンパク質の爆発パターンがどこまで似通っているか、一目でわかるようになるのです。
すると驚くことに、一見そっくりと思っていたタンパク質でも爆発フットプリントがはっきり分かれて、別々のクラスターを作る例が続出したのです。
まさに双子が遠目には見分けがつかないけれど、よく見ると細かい表情や仕草の違いで区別できるようになる、そんな感覚に近いかもしれません。
しかもこの結果は、「分子が持つわずかな構造の違いが、爆発の瞬間にかなり大きく影響を与える」という点を示しています。
たとえば“コンパクトに折りたたまれた形”と“伸び伸びと広がった形”がわずかに違うだけでも、破片の飛び散り方が変わってくる。
しかも“まったく同じアミノ酸配列で折りたたみがごく一部だけ異なる”ようなケースでも、爆発後のパターンだけで見分けがついたのです。
こうした結果は、従来の手法ではなかなか見抜きにくい微妙な差を、何と“分子が壊れる様子”から捉えることができたことを意味します。
なぜこれが革新的といえるのか?
それは、結晶化や複雑な測定準備をしなくても、たとえタンパク質が壊れてしまっても、その壊れ方を正確に観察すれば、元の構造情報を引き出せるかもしれないからです。
今までなら「分子が壊れたらデータは終わり」という発想が当たり前でした。
ところがこの研究は、「壊れる瞬間」をデータとして活用するという逆転の発想がどれほど有用かを示しました。
これによって、従来法では扱いにくい柔軟な分子や一時的な構造変化を、クーロン爆発のパターンだけで見極められる未来が来るかもしれません。
いわば、最初は“花火が終わると消えてしまう”と考えられていたのに、火花の軌道から玉の組成や火薬の配合を推定する—そんな離れ業が本当にできるようになる可能性を示した点が、今回の最大の見どころです。
壊れる瞬間から逆算する、分子の真実
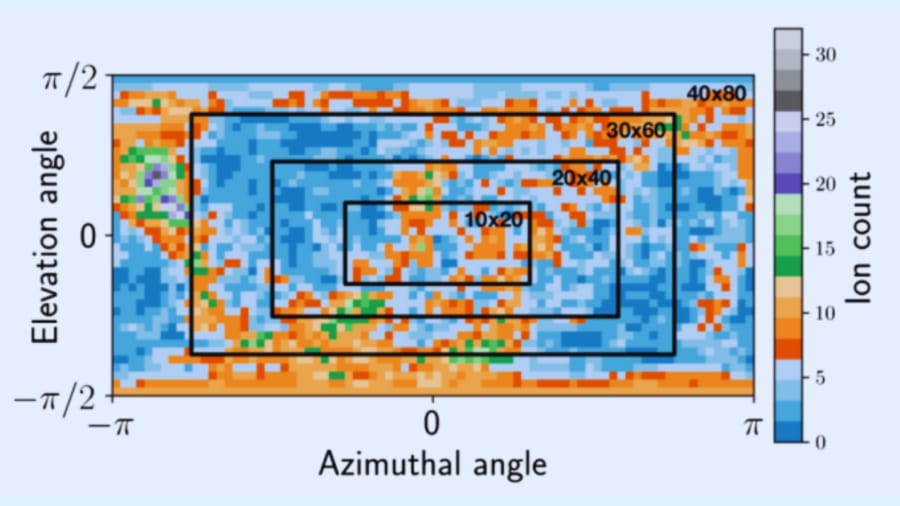
今回の研究で特に興味深いのは、“一瞬で壊れてしまうタンパク質”からでも、壊れる瞬間のデータを解析すれば細かな構造差までわかるかもしれない、という逆転の発想です。
たとえば、通常であれば「分子が壊れたら終わり」と考えがちです。
しかし、クーロン爆発の飛び散り方がきちんとしたパターンを示すなら、それを正しく読み取ることで、むしろ爆発前の姿—つまりタンパク質がどう折りたたまれていたか—を推定できる可能性があるわけです。
しかも今回、アミノ酸配列こそ同じでも、折りたたみ方や複合体の有無がほんの少し違うだけで爆発フットプリントが変化することが確認されました。
これは実験環境や分析手順をさらに工夫すれば、もっと微細な分子変化まで判別できるかもしれないという期待につながります。
また、実際の実験に置きかえて考えると、ほんの一部分の角度しか検出器でカバーできなくても、意外と情報が失われずに識別できるというシミュレーション結果も示唆的です。
もしこの方式を本格的に適用できるようになれば、結晶化できないタンパク質の研究や、一時的な構造変化をとらえる研究で威力を発揮するかもしれません。
たとえばタンパク質が反応途中でどんなふうに形を変えるのか、爆発フットプリントの違いでリアルタイムに見分ける、といった応用も考えられそうです。
一方で、この研究はあくまでシミュレーションに基づいており、実際のXFELを使った実験でどこまで同じ精度が出せるか、タンパク質の向きをどう把握するか、といった課題は残ります。
ただ、最近は外部電場で分子の姿勢をある程度そろえる技術や、タンパク質内の特定元素(硫黄など)をタグのように利用する手法も提案されています。
そういった技術とクーロン爆発のパターン解析が組み合わされば、いずれは実験室レベルでも「爆発フットプリントだけで分子の全貌を推定する」という場面が来るかもしれません。
さらに、コンピュータでの構造予測ソフト(たとえばAlphaFoldなど)が進歩している今、実験結果を機械学習で解析して補完するのも有力です。
もし爆発フットプリントを何千、何万と集めれば、そのデータを学習させることで、未知のタンパク質がどんな立体構造を取りやすいか自動推定する…といった道も開けるでしょう。
つまり従来の「結晶化してX線回折を解析する」という手順とはまったく違う形で、生体分子の構造に挑む未来が見えてきます。
こうした点を踏まえると、今回の結果は単なる「爆発シミュレーションの成功」という枠を超えて、“壊れる瞬間”を活かすという新たな考え方を打ち出した、といえます。
結晶化という大きな壁、装置の制約、時間分解や配向などさまざまなハードルを乗り越える糸口として、クーロン爆発の解析が有望な選択肢となることを示唆しているのです。
今後、実験面での改良や理論的モデルの進化に伴い、この手法がどこまで一般的なツールになっていくのかが注目されます。
タンパク質を“爆発させる”という、一見奇抜な発想が、構造生物学の世界を大きく変えるかもしれません。
元論文
Protein Structure Classification Based on X-Ray-Laser-Induced Coulomb Explosion
https://doi.org/10.1103/PhysRevLett.134.128403
ライター
川勝康弘: ナゾロジー副編集長。 大学で研究生活を送ること10年と少し。 小説家としての活動履歴あり。 専門は生物学ですが、量子力学・社会学・医学・薬学なども担当します。 日々の記事作成は可能な限り、一次資料たる論文を元にするよう心がけています。 夢は最新科学をまとめて小学生用に本にすること。
編集者
ナゾロジー 編集部